De basisbeginselen van stolling
Bloedstolling
De bloedstolling kan theoretisch in drie delen worden gesplitst. Het eerste deel betreft het proces van primaire hemostase, waarbij de trombocyten plakken aan de vaatwand en een bloedprop vormen. Hier na wordt een stevig bloedstolsel met fibrine gevormd met hulp van de stollingsfactoren. Ten slotte kan enige tijd nadat de vaatwand is gerepareerd, het bloedstolsel worden opgeruimd. Dit is het proces van fibrinolyse. In de praktijk kunnen deze processen simultaan verlopen. De drie belangrijkste spelers bij de bloedstolling zijn de vaatwand en het endotheel, de trombocyt en de (anti)stollingsfactoren.
Vaatwand en endotheel
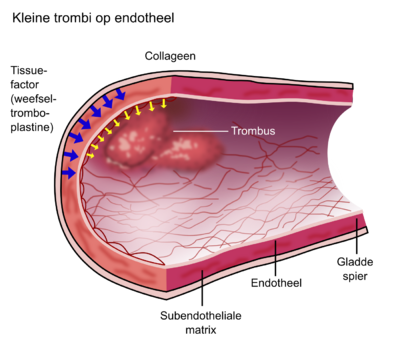
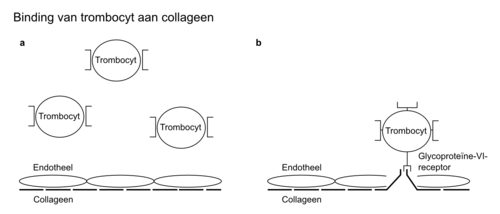
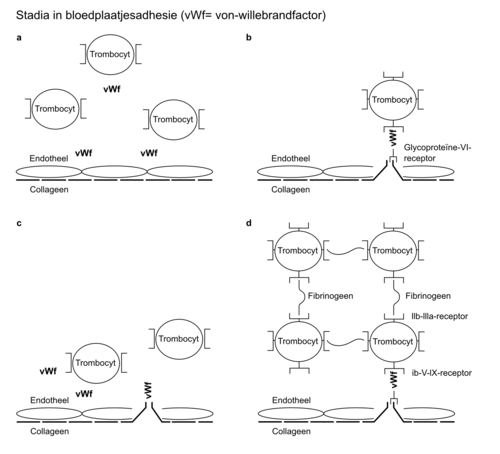
De primaire hemostase is het begin van de bloedstolling en vindt zijn oorsprong in een defect in de vaatwand. Bij het ontstaan van een defect in de vaat wand komen structuren die onder het endotheel liggen, waarvan vooral collageen en ook fibronectine van belang zijn, in aanraking met bloed (figuur 1). Collageen bindt aan de bloedplaatjesreceptor glycoproteïne-VI. Voorts bindt glycoproteïne-Ib-V-IX-receptor, dat op de celmembraan van de trombocyt zit met de aan collageen gebonden von-Willebrandfactor (vWf). Hierdoor ontstaat een directe verbinding tussen het subendotheel (collageen) en de trombocyt (Ib-V-IX-receptor), waarbij de vWf een ligand vormt. Adhesie van collageen aan glycoproteïne VI resulteert in activatie van intracellulaire signaaltransductiepaden in de trombocyt. Dit leidt tot een vormverandering (shape change) van de geactiveerde trombocyt. Hierdoor komt een andere receptor van de trombocyt (glycoproteïne-IIb-IIIa-receptor) door omkering van de plaatjesmembraan (flip-flop) aan het oppervlak van de trombocyt. Vervolgens kunnen er door fibrinogeen of andere eiwitten, zoals vitronec tine en trombospondine, verbindingen worden gemaakt met andere trombocyten (figuur 2). Dit leidt tot aggregatie van trombocyten.
Deficiënties van elk van de genoemde receptoren of liganden leiden tot een verminderde functie van de primaire hemostase en ten gevolge daarvan een verhoogde bloedingsneiging. De ziekte van von Willebrand is hierbij de meest voorkomende aandoening. Deze autosomaal dominante aando ening wordt veroorzaakt door een tekort of afwezigheid van de vWf. Hierdoor wordt minder of geen verbinding gemaakt tussen het beschadigde endotheel en de trombocyt. Dit geeft een verhoogde bloedingsneiging, daarbij de ernst van de aandoening afhankelijk is van de concentratie van de vWf. De verhoogde bloedingsneiging uit zich met name in slijmvliesbloedingen (tandvlees, hevige menstr uaties). Voorts is de vWf het carrier-eiwit van factor VIII. Hierdoor is bij een ernstig tekort van de vWf ook factor VIII verlaagd. Dit resulteert dan naast een afwijkende primaire hemostase ook in een gestoorde fibrinevorming.
De trombocyt
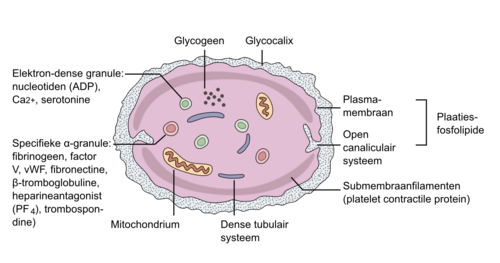
De trombocyt heeft aan het oppervlak een grote hoeveelheid receptoren, waar van de glycoproteïne-IIb-IIIa-receptor het grootst in aantal is. In de trombocyt liggen verschillende granulae. De twee belangrijkste voor de primaire hemostase zijn de dense en de α-granula. Tijdens het activeren van de bloedplaatjes treedt er een scala van biochemische reacties in het bloedplaatje op. De inhoud van de granula komt bij deze act ivatie vrij. Verschillende stoffen die zich in granula bevinden, worden naar buiten gestoten. Vrijwel al deze stoffen leiden tot een versterking van de bloedplaat jesactivatie, vooral omdat zich op de plaatjesmembraan receptoren bevinden voor de meeste van deze moleculen. Belangrijke voorbeelden zijn adenosinedifosfaat (ADP), collageen, adrenaline en trombine (zie figuur 3).
Bij afwijkingen in de granulae kan een tekort aan deze factoren optreden en dit leidt tot een storage pool disease. De primaire hemostase is hierbij gestoord. Door meting van plaatjesfactor 4 (PF4) en ß-tromboglobuline (BTG) in zowel bloedplaatjes als plasma en meting van serotonine (5-HT) in plasma kan een storage pool disease worden vast gesteld. Bij een storage pool disease van de α-granula is er een verlaagde waarde van PF4 en BTG in plaatjes. De waarden in plasma dienen dan ook laag te zijn (als deze waarde verhoogd is bij een lage plaatjesconcentratie, wijst dit op invitroactivatie). Bij een verlaging van 5-HT in plasma is er sprake van een storage pool disease van de dense granula. Een andere belangrijke biochemische reactie is de omzetting van arachidonzuur uit de bloedplaatjesmembraan in tromboxaan-A 2. Tromboxaan-A2 kan weer andere bloedplaatjes activeren, die op hun beurt een bijdrage kunnen leveren aan de trombocytenprop. Tevens heeft tromboxaan-A2 een sterk vaatvernauwend effect. Vaat vernauwing is een belangrijk onderdeel in de primaire hemostase. De omzetting van arachidonzuur in tromboxaan-A2 gebeurt onder invloed van het enzym cyclo-oxygenase (COX). Dit cyclo-oxygenase wordt volledig en irreversibel geremd door acetylsalicylzuur. Clopidogrel en prasugrel remmen een alternatieve act iveringsroute van de trombocyt door de ADP-receptor te blokkeren. Op deze wijze wordt de trombocytenaggregatie eveneens irreversibel geremd.
Fibrinestolselvorming
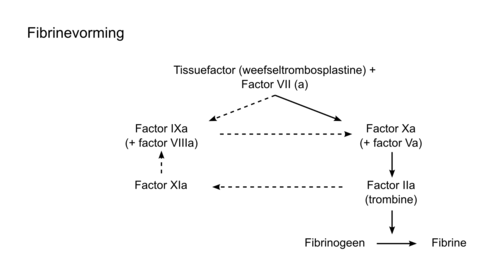
Nadat door de trombocyten een bloedprop is gevormd, zal in een volgende fase het bloedstolsel moeten worden verstevigd. Hiervoor is de vorming van het onoplosbare fibrine nodig (zie figuur 4). Fibrine ontstaat uit fibrinogeen onder invloed van trombine (factor IIa). Trombine is de geactiveerde vorm van de stollingsfactor protrombine (factor II).
Bloedstolling begint als het membraaneiwit tissuefactor (of weefseltromboplastine) in aanraking komt met het stromende bloed. Tissuefactor is in normale omst andigheden gelokaliseerd onder het endotheel in de media en adventit ia van de vaatwand en komt normaal dus niet in contact met bloed. Als er een defect in de vaatwand ontstaat, treedt het bloed buiten de bloedbaan en komt dan in aanraking met de onder het endotheel gelegen tissuefactor. Tissuefactor vormt samen met spoortjes geactiveerde factor VII (factor VIIa) uit het bloed een complex en bindt tevens aan ongeactiveerde stollingsfactor VII uit het bloed, waarop verdere vorming van factor VIIa plaatsvindt. Het aldus gevormde tissuefactor/factor VIIa-complex bindt aan factor X en activeert factor X tot factor Xa. Dit trivalente complex van tissuefactor/factor VIIa/factor Xa (ook het tenasecomplex genoemd) kan op zijn beurt met behulp van stollingsfactor V het protrombine (factor II) omzetten in trombine (factor IIa). Deze laatste reactie gebeurt ook weer door vorming van een complex bestaande uit factor II (protrombine), factor Xa en factor V (protrombinasecomplex), waarbij tevens een geschikt fosfolipidenoppervlak (bijvoorbeeld de geactiveerde trombocytenmembraan) essentieel is. Zoals eerder vermeld, zorgt factor IIa tenslotte voor omzetting van fibrinogeen in fibrine. Naast deze belangr ijkste route van het stollingssysteem zijn er twee ‘versterkingslussen’.
In de eerste plaats kan het tissuefactor/factor VIIa-complex ook indirect factor X activeren via activatie van factor IX (tot factor IXa). Met behulp van de stollingsfactor VIII kan factor IXa extra factor X activeren tot factor Xa. Het belang van deze route wordt het best geïllustreerd aan de hand van het feit dat patiënten met een aangeboren tekort of soms zelfs volledige afwezigheid van factor VIII of factor IX (respectievelijk hemofilie-A of hemofilie-B) een ernstige bloedingsneiging hebben. Een tweede versterkingslus best aat uit de act ivering van factor XI door het gevormde trombine. Factor XIa kan factor IX activeren en via factor X resulteert dit vervolgens in protrombineactivering. Trombine stimuleert op deze wijze dus ook zijn eigen vorming. Om stevigheid te verkrijgen moeten dwarsverbanden worden gevormd tussen de ontstane fibrinevezels. Deze cross-linking van fibrinepolymeren gebeurt onder invloed van de transglutaminasefactor XIIIa, die ontstaat door activatie van de zymogene factor XIII onder invloed van trombine. Vrijwel alle stollingsfactoren worden door de lever geproduceerd. Dit betekent dan ook dat er bij een verminderde werking van de lever verlaagde concentraties van stollingsfactoren in het bloed zullen zijn en dit kan leiden tot een stollingsstoornis. Een aantal stollingsfactoren kan pas actief worden als een van de aminozuren, een glut aminezuur, wordt gecarboxyleerd. Deze carboxylering vindt plaats onder invloed van vitamine-K en is een essentiële voorwaarde voor het vermogen van deze stollingsfactoren om fosfolipiden te binden. Het betreft de vitamine-K afhankelijke stollingsfactoren II, VII, IX en X. Hierdoor zullen er bij een tekort aan vitamine-K verlaagde functioneel actieve concentraties van deze factoren ontstaan. Dit leidt tot een verminderde werking van de bloedstolling.
Remmers van de bloedstolling
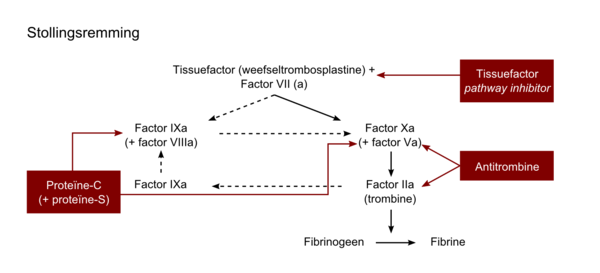
Het bloedstollingssysteem is een zeer krachtig werkend systeem dat in zeer korte tijd het bloed moet kunnen laten stollen. De potentie van het systeem wordt misschien wel het best geïllustreerd door het feit dat de factoren die aanwezig zijn in enkele milliliters bloed, voldoende zijn om het volledige circulerende bloed te laten stollen. Aangezien te veel stolling ongewenst is en kan leiden tot trombose, moet dit systeem strak worden gereguleerd. Hiertoe bestaat een systeem van stollingsremmers. Stollingsremmers zijn net als stollingsfactoren eiwit ten die het stollingssysteem op diverse plaatsen kunnen remmen. Fysiologische stollingsremming vindt plaats op drie niveaus (figuur 6).
1. Remming van het tissuefactor/factor VIIa-complex door:
- Tissue Factor Pathway Inhibitor (TFPI)
- Remming van de cofactoren V en VIII door het geactiveerde proteïne C-systeem
- Remming van factor Xa en IIa (trombine) door antitrombine
2. Antitrombine is een serineproteaseremmer die bindt aan het reactieve centrum van de geactiveerde factoren X en II, waardoor deze volledig en irreversibel worden geremd. Deze binding is enzymatisch nogal traag, behalve in aanwezigheid van heparineachtige stoffen waarop de katalytische efficiënt ie van dit proces duizendvoudig toeneemt. Hierop berust dan ook de farmacologische werking van heparine(derivaten).
3. De belangrijke cofactoren, factor Va en factor VIIIa, worden proteolytisch afgebroken door een andere remmer, geactiveerd proteïne-C. Activatie van proteïne-C geschiedt door het aan het endotheeloppervlak aanwezige trombomoduline, dat weer wordt geactiveerd door trombine. Geactiveerd proteïne-C heeft om zijn werk goed uit te kunnen oefenen zelf ook een cofactor nodig, namelijk proteïne-S.
Fibrinolyse
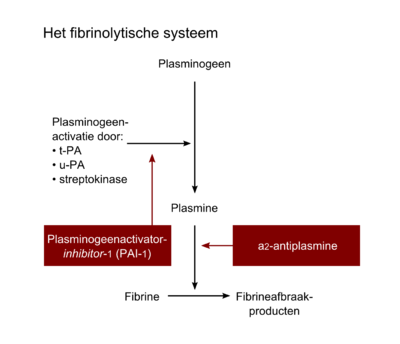
Voor het opruimen van het fibrinestolsel zorgt het fibrinolytische systeem (figgur 7). Het belangrijkste onderdeel is het eiwit plasmine, dat in staat is het onoplosbare fibrine om te zet ten in oplosbare fibrineafbraakproducten. Plasmine is een geactiveerde vorm van een circulerend zymogeen, het plasminogeen. De omzetting van het inactieve plasminogeen in het actieve plasmine gebeurt onder invloed van de plasminogeenactivatoren. Dit zijn eiwitten die zich in relatief hoge concentraties in de endotheelcellen bevinden en die zo nodig daar uit kunnen worden vrijgemaakt. De twee belangrijkste fysiologische plasminogeenactivatoren zijn weefsel type plasminogeenactivator (tissue type plasminogen activator (t-PA) en urokinasetype-plasminogeenactivator (u-PA).
Remming van de fibrinolyse vindt plaats op twee niveaus:
- Het gevormde plasmine wordt direct geremd door de serineproteaseremmer α2-antiplasmine (en andere proteaseremmers). Dit α2-antiplasmine wordt ook onder invloed van de eerdergenoemde factor XIIIa in het stolsel ingevlochten, waardoor in het zich vormende fibrinenetwerk een zekere mate van bescherming tegen fibrinolyse wordt ingebouwd.
- Efficiënte remming van fibrinolyse kan ook geschieden door remming van de plasminogeenactivatoren, onder invloed van de remmer plasminogeenactivator-inhibitor type 1 (PAI-1).