Interpretatie stollingsonderzoek
Interpretatie van stollingsonderzoek
Diagnostiek bij stollingsstoornissen
Stollingsstoornis uiten zich door het optreden van bloedingen. Vooral het optreden van bloedingen op verschillende plaatsen en onder verschillende omstandigheden geeft een verdenking op een stollingsstoornis. Bij een patiënt die verdacht wordt van een stollingsstoornis is, alle ingewikkelde en gevoelige laboratoriummethoden ten spijt, de anamnese van het belangrijkste. Spontane bloedingen, bloedingen na relatief gering trauma of excessief bloedverlies na kleine chirurgische en tandheelkundige ingrepen kunnen wijzen op een stoornis in de hemostase. Anderzijds is bij een patiënt die in het verleden bijvoorbeeld kiesextracties of een amandeloperatie heeft ondergaan, zonder dat daarbij bloedingscomplicaties zijn opgetreden, de aanwezigheid van een aangeboren stollingsdefect minder waarschijnlijk. Aan de lokalisatie van de bloeding is soms vast te stellen waar het stollingsdefect zich bevindt. Afwijkingen in de primaire hemostase kenmerken zich vooral door het optreden van slijmvliesbloedingen, zoals een neusbloeding of een darmbloeding. Het optreden van petechiën (kleine puntvormige bloedinkjes in de huid) past vrijwel exclusief bij een ernstige trombocytopenie. Echter een patiënt met een (ernstige) stoornis in de fibrinevorming zal zich presenteren met spier- en gewrichtsbloedingen of (gelukkig relatief zeldzaam) een hersenbloeding. Uiteindelijk is met laboratoriumonderzoek de aanwezigheid en aard van de stollingsstoornis goed vast te stellen. Gezien de veelheid van factoren en componenten die betrokken zijn bij een goed functioneren van de bloedstolling, zijn screenende testen noodzakelijk.
Stollingstesten primaire hemostase
Voor het screenen van de primaire hemostase is in de meeste gevallen het bepalen van het aantal trombocyten in het bloed voldoende en door middel van de zogenaamde ‘bloedingstijd’ nagaan of deze bloedplaatjes goed functioneren. De bloedingstijd is een test waarbij met een scherp mesje een minuscuul krasje in de huid wordt gezet en wordt gemeten hoe lang het duurt voordat de bloeding gestelpt is. Door de aard van de test is deze speciaal geschikt om het functioneren van de primaire hemostase na te gaan. Indien de bloedingstijd verlengd is, is verder onderzoek aangewezen. Zo kan in dat geval bijvoorbeeld het gehalte aan von-Willebrand-factor worden bepaald of kan de bloedplaatjesaggregatie in bij de patiënt afgenomen bloed, in het laboratorium worden nagebootst. Men dient zich wel te realiseren dat de sensitiviteit en specificiteit van de bloedingstijdbepaling beperkt is. Het is niet zinvol een bloedingstijdtest te doen als het aantal trombocyten kleiner is dan 50x109/l.
Aggregatieonderzoek
Bloedplaatjes uit het bloed van de patiënt worden bij dit onderzoek geïsoleerd en na toevoeging van diverse agonisten in een aggregometer onderzocht om te kijken of er een goede bloedplaatjesaggregatie aanwezig is (figuur 1). Als de bloedingstijd verlengd is en het aggregatieonderzoek geen conclusie mogelijk maakt, kan een ‘storage pool disease’ worden vastgesteld door meting van plaatjesfactor IV (PF-4) en ß-tromboglobuline (ß-TG) in zowel bloedplaatjes als plasma en meting van serotonine (5-HT) in plasma. Bij een ‘storage pool disease’ van de α-granula is er een verlaagde waarde van ß-TG en PF-4 in plaatjes. De waarden in plasma dienen dan ook laag te zijn (als deze verhoogd is bij een lage plaatjesconcentratie wijst dit op in-vitro-activatie). Bij een verlaging van 5-HT in plasma is er sprake van een ‘storage pool disease’ van de dense granula. Immunocytometrie met antistoffen tegen oppervlakte-antigenen van bloedplaatjes kan een diagnose van congenitale trombocytopathie bevestigen.
Stollingstesten fibrinevorming
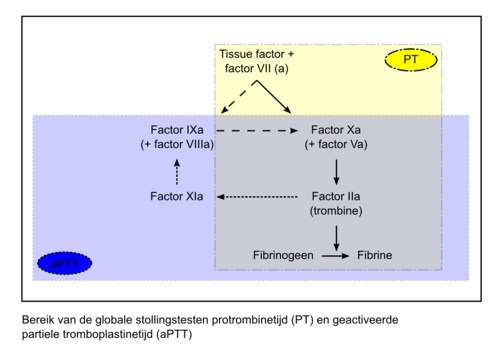
Fibrinevorming is te meten door de werking van dit systeem te imiteren in bij de patiënt afgenomen bloed. Bij dit bloed wordt een kleine hoeveelheid van een bloedstollingsactivator (bijvoorbeeld tissue factor) gemengd en dan wordt gemeten wordt hoe lang het duurt tot zich een fibrinestolsel heeft gevormd. Over het algemeen is met twee testen een goede werking van vrijwel het gehele stollingssysteem na te gaan. Het gaat dan om 2 testen, namelijk de zogenaamde ‘protrombinetijd’ (PT) en de ‘geactiveerde partiële tromboplastinetijd’ (aPTT). Bij een abnormale uitslag van de test kan worden nagegaan waar zich in het stollingssysteem een afwijking bevindt (figuur 2 en tabel 1).
Een abnormale testuitslag van de aPTT en/of de PT wordt gevolgd door meer uitgebreid stollingsonderzoek om de afwijking precies vast te stellen. De differentiële uitslag van de aPTT en PT kunnen richtinggevend zijn voor verder onderzoek. Tussen verschillende laboratoria kunnen grote verschillen in testuitslagen bestaan, onder andere door gebruik van verschillende reagentia. In het geval van de PT is dit van speciaal belang, omdat deze test wordt gebruikt om de intensiteit van antistollingsbehandeling met vitamine-K-antagonisten (coumarine derivaten) te monitoren. Daarom wordt de PT voor deze situatie met hulp van een correctiefactor (ISI), afhankelijk van het gebruikte reagens, uitgedrukt in ‘International Normalized Ratio’ (INR) die wel tussen verschillende laboratoria kan worden vergeleken.
| aPTT verlengd, PT normaal |
|---|
|
| aPTT normaal, PT verlengd |
|
| aPTT verlengd en PT verlengd |
|
|
* een factor XII-deficiëntie leidt niet tot een verhoogde bloedingsneiging |